به گزارش زیستنا به نقل از Rice University، دانشمندان با القای مسیری «غیرمتعارف» در سلولها کاری کردند تا سلولها، خود دارو تولید کنند. محققان به لطف پرنده کمیاب اکراس کاکلی (Crested ibis) سرنخی را یافتند که میتواند روزی به بدن ما در ساخت داروهای بهتر کمک کند.
این پرنده تنها گونهای است که بهطور طبیعی آنزیمی تولید میکند که قادر به تولید یک آمینواسید غیرمتعارف است؛ یعنی یکی از ۲۰ مورد ضروری برای رمزدهی اغلب پروتئینها نیست.
این موضوع که چنین پدیدهای وجود دارد کشفی است که از طریق مقایسه رایانهای پایگاههای داده ژنوم انجام شده است. این امر ثابت میکند که آنزیم فوق میتواند در بافت سلولهای زنده کار کند، حتی اگر دانشمندان ندانند که این آنزیم چه کاری برای آن پرنده انجام میدهد.
اما آنها ایده بسیار خوبی دارند که این آنزیم چه کاری میتواند برای ما انجام دهد.
هان شیائو (Han Xiao)، شیمیدان دانشگاه رایس، پیتر وولینز (Peter Wolynes)، فیزیکدان نظری و همکارانشان مطالعهای جدید انجام دادهاند. این مطالعه نشان میدهد که آمینواسید سولفوتیروزین (Sulfotyrosine) یا بهاختصار sTyr واحد ساختاری کلیدی برای برنامهریزی سلولهای زنده است که پروتئینهای درمانی را بیان میکنند. sTyr شکل تغییریافتهای از آمینواسید استاندارد تیروزین است. این ماده بهطور بالقوه میتواند به سلولها اجازه دهد تا بهعنوان حسگرهایی عمل کنند که محیطشان را پایش میکنند و با تیمار لازم پاسخ میدهند.
تقلید از توانایی اکراس برای ساخت sTyr و ترکیب آن در پروتئینها نیازمند اصلاح DNA سلول با کدونی (Codon) جهشیافته است. این کدون بهنوبه خود آنزیم ترانسفرازی موسوم به سولفوترانسفراز ۱C1 یا Sulfotransferase 1C1 موجود در این پرنده را میسازد. این آنزیم تولید sTyr، بخش شناسایی ضروری در انواع برهمکنشهای زیستمولکولی را کاتالیز میکند.
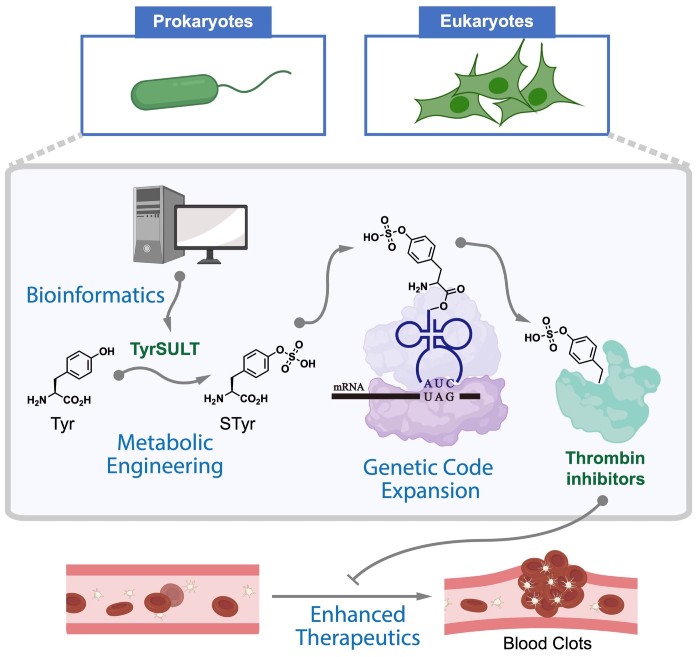
مطالعه اثبات مفهوم برای نخستین بار سلولهای پستاندارانی را تولید کرد که sTyr را تولید میکردند. آزمایشگاه شیائو طی آزمایشی سلولهایی را ساخت که قدرت مهارکنندههای ترومبین را افزایش میدهند. مهارکنندههای ترومبین ضد انعقادهایی هستند که برای جلوگیری از لخته شدن خون استفاده میشوند. این مطالعه در Nature Communications منتشر شده است.
شیائو گفت: «در طبیعت، بیشتر گونههای ما با ۲۰ واحد ساختاری متعارف ساخته شدهاند.» وی ادامه داد: «اگر میخواهید یک واحد ساختاری اضافی را بیفزایید، باید به چگونگی ساخت آن فکر کنید. ما آن مشکل را حل کردیم: میتوانیم از سلول بخواهیم آن را بسازد.»
«اما پسازآن ما باید دستگاه ترجمه را وادار کنیم آن را تشخیص دهد و یک کدون ویژه برای رمزدهی این واحد ساختاری جدید داشته باشیم.» وی افزود: «با این مطالعه، ما هر سه مورد از این الزامات را تأمین کردهایم.»
شیائو در سال ۲۰۱۹ کمکهزینهای از انستیتو ملی بهداشت دریافت کرد تا بررسی کند که آیا میتوان سلولها را برای ساخت موادی با آمینواسیدهای اضافی برنامهریزی کرد یا خیر. مطالعه جدید پیشرفت چشمگیر این آزمایشگاه را نشان میدهد.
تاکنون، دانشمندان آمینواسیدهای غیرمتعارف ساختهشده به روش شیمیایی را به سلولها وارد کردند. به گفته شیائو، وادار کردن سلول برای انجام این کار بسیار کارآمدتر است، اما این امر نیازمند کشف آنزیم ترانسفراز جدیدی بود که دارای جایگاههایی برای تیروزین باشد تا بتواند به سولفات متصل شود. این ترکیب قفل و کلید میتواند بهعنوان پایهای برای انواع کاتالیزورها استفاده شود.
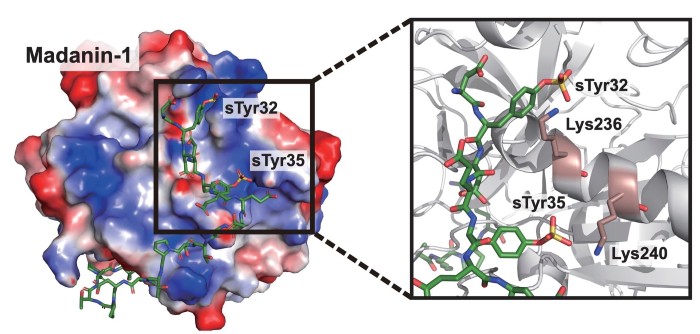
او گفت: «اکنون، از طریق این راهکار جدید برای اصلاح پروتئینها، میتوانیم ساختار پروتئین و عملکرد آن را کاملاً تغییر دهیم.» وی اضافه کرد: «ما برای مدلهای مهارکنندههای ترومبین خود نشان دادیم که قرار دادن یک واحد ساختاری غیرطبیعی در دارو میتواند این دارو را بسیار قویتر کند.»
ارزش داشت تا بررسی شود که آیا طبیعت زودتر از آنها کدون مفیدی را ایجاد کرده است یا خیر. برای این کار، شیائو از وولینز، یکی از مدیران مرکز فیزیک زیستی نظری کمک گرفت. آزمایشگاه وولینز پایگاههای داده ژنوم را مقایسه کرد و سولفوترانسفراز ۱C1 را در اکراس پیدا کرد.
آزمایشگاه شیائو از یک کدون توقف امبر (Amber Stop Codon) جهشیافته، یک گروه سه نوکلئوتیدی از اوراسیل، آدنین و گوانین برای رمزدهی سولفوترانسفراز مورد نظر استفاده کرد. در نتیجه رده سلولی پستانداران کاملاً مستقلی ایجاد شد که قادر به تولید sTyr و وارد کردن آن با دقت زیاد در پروتئینها بود.
شیائو گفت: «ما خوششانس بودیم. اکراس تنها گونهای است که این کار را انجام میدهد که این موضوع با جستجوی توالی شباهت اطلاعات ژنومی کشف شد. پسازآن، ما این پرسش را طرح کردیم که آیا آنها میتوانند دریابند که چرا این آنزیم تیروزین را تشخیص میدهد اما سولفوترانسفراز انسانی ما نمیتواند.»
گروه وولینز از AlphaFold2 استفاده کرد. این برنامه یک برنامه هوش مصنوعی است که بهوسیله سیستم Alphabet/ DeepMind گوگل توسعه یافته و ساختار پروتئینها را پیشبینی میکند.
پژوهشگران انتظار دارند از ترکیب بیوانفورماتیک و غربالگری پیشرفته رایانهای برای تولید یک کتابخانه از آمینواسیدهای غیرمتعارف زیست ساختهشده استفاده کنند.
منبع: Rice University
Journal Reference:
Chen, Yuda, Shikai Jin, Mengxi Zhang, Yu Hu, Kuan-Lin Wu, Anna Chung, Shichao Wang, et al. “Unleashing the Potential of Noncanonical Amino Acid Biosynthesis to Create Cells with Precision Tyrosine Sulfation.” Nature Communications ۱۳, no. 1 (September 16, 2022): 5434. https://doi.org/10.1038/s41467-022-33111-4.

